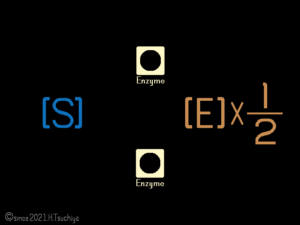【76】酵素反応と化学平衡

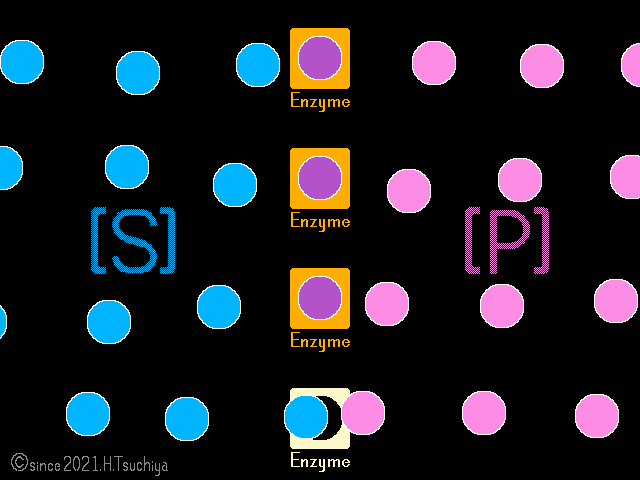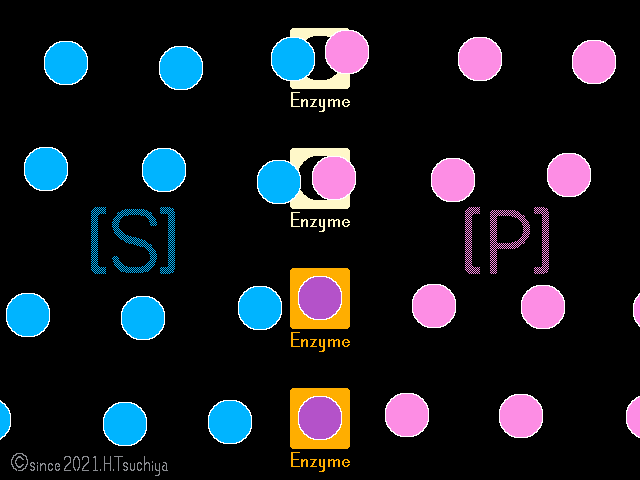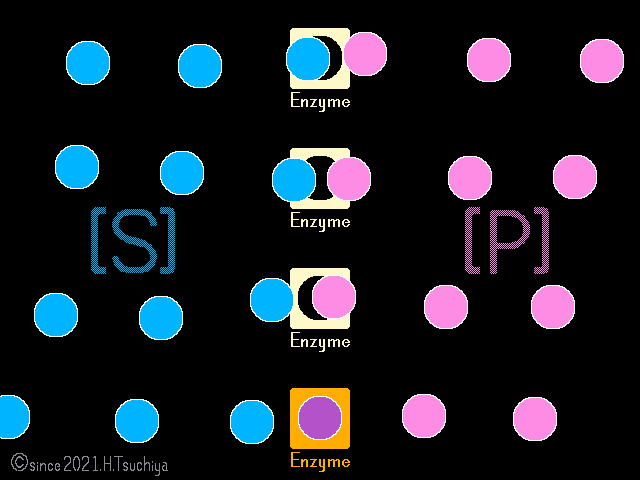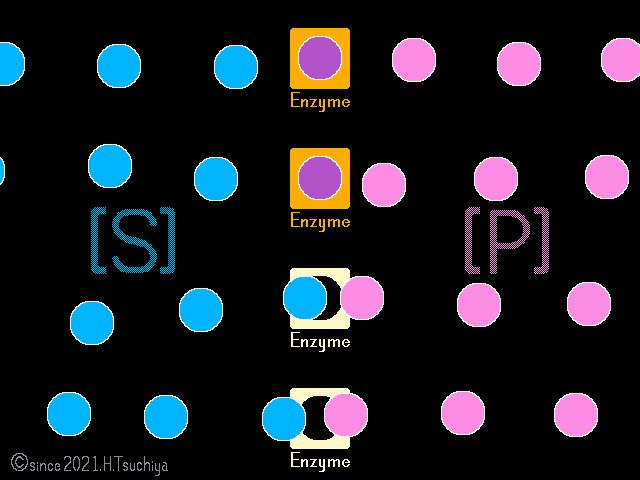
酵素反応が進むと、時間に伴って生成物量[濃度]が上昇するけれども、徐々に上昇は緩やかになり、やがて止まる。
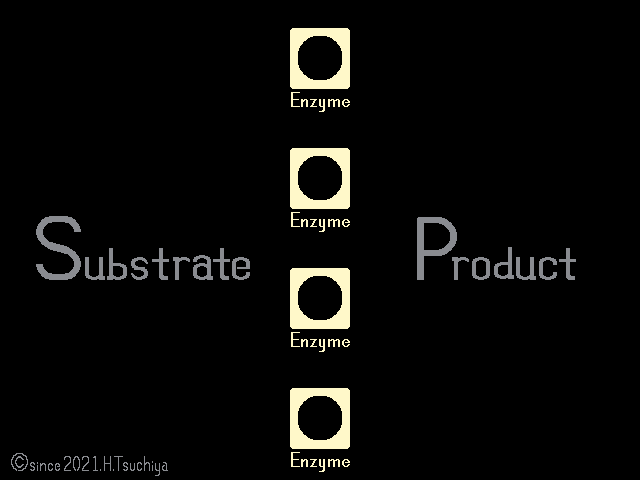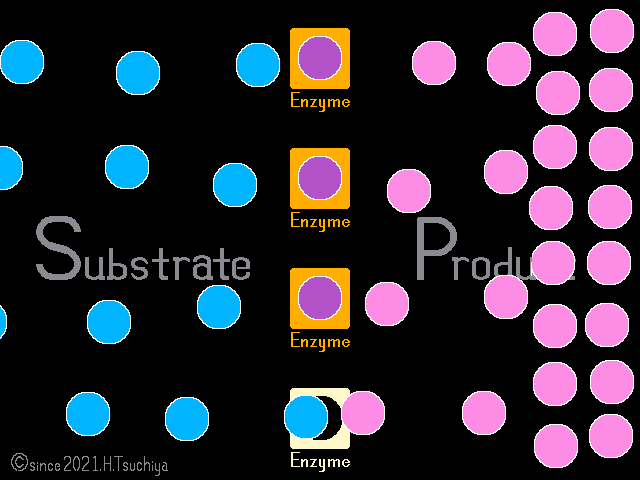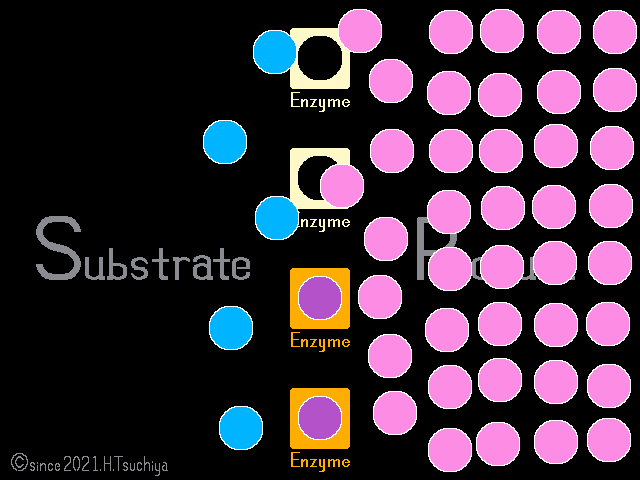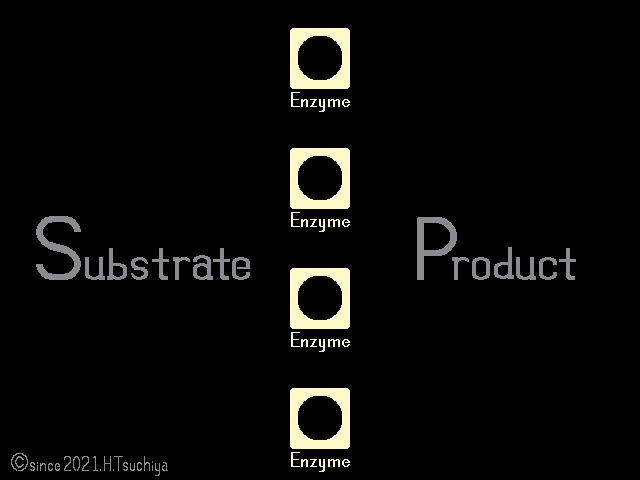
一見すると反応が停止した様に見えるけれど、可逆的な酵素反応では、正反応(基質→生成物)と逆反応(基質←生成物)が同時に進行している。
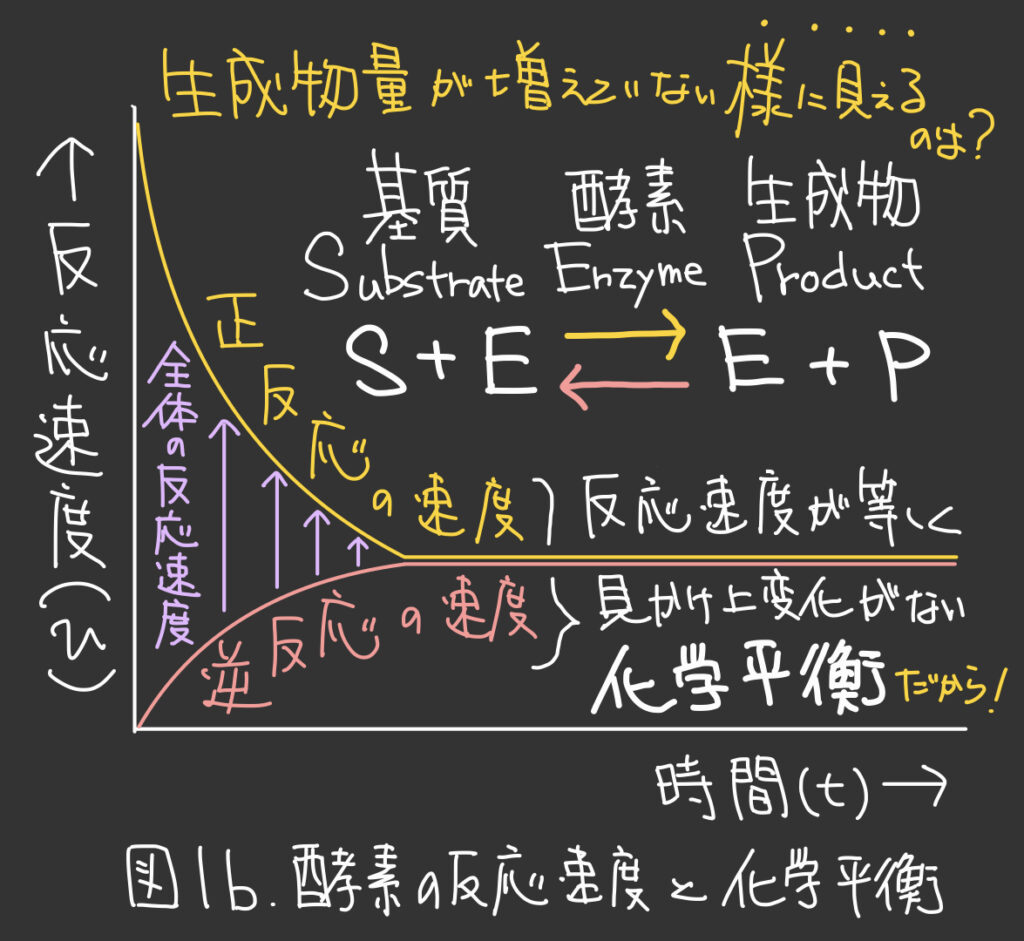
化学反応の速度は基質の濃度に比例するので、反応初期は基質濃度が高いために〈正反応の速度〉が〈逆反応の速度〉を上回る。
反応が進むと、基質濃度が低くなるので〈正反応の速度〉は低下し、一方で生成物濃度が高くなるので〈逆反応の速度〉は上昇する。
やがて、〈正反応の速度〉と〈逆反応の速度〉が等しくなると、反応が停止した様に見える化学平衡の状態になる。
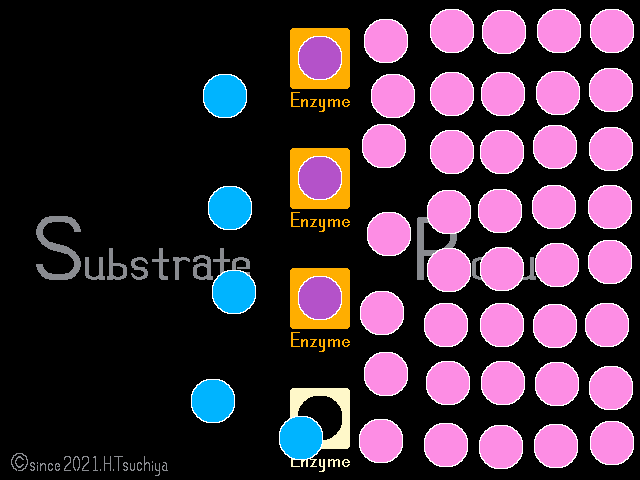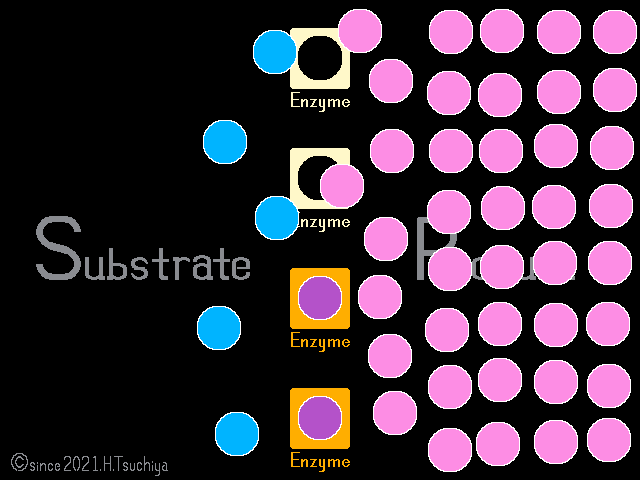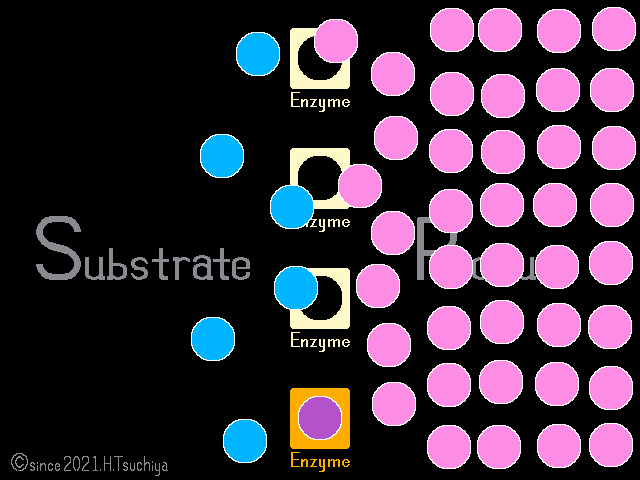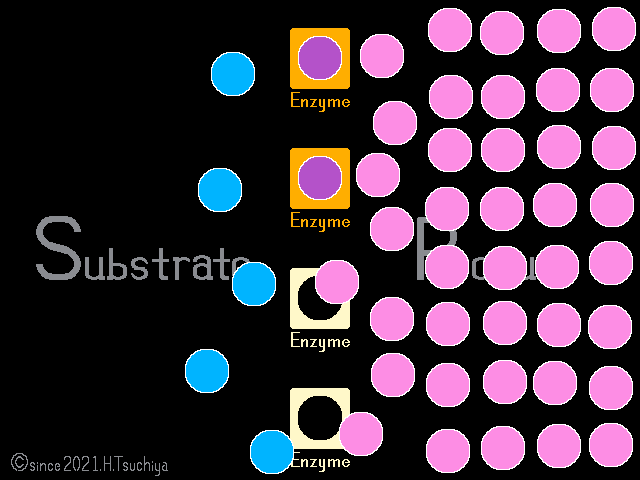
平衡状態に達しても、基質や生成物の濃度が変化すれば〈正反応の速度〉と〈逆反応の速度〉のバランスが崩れて、化学平衡は解消する。
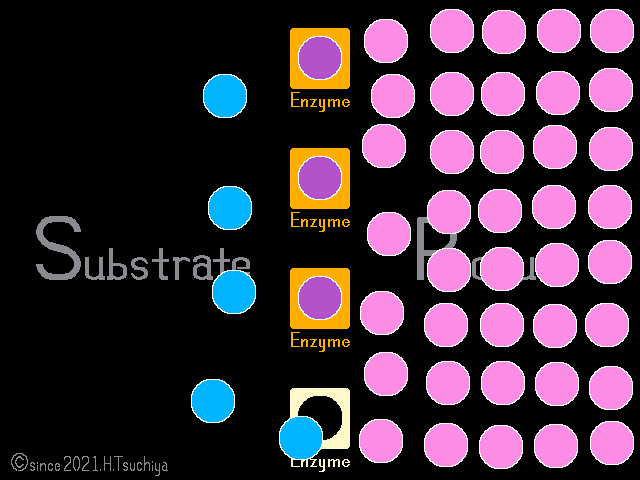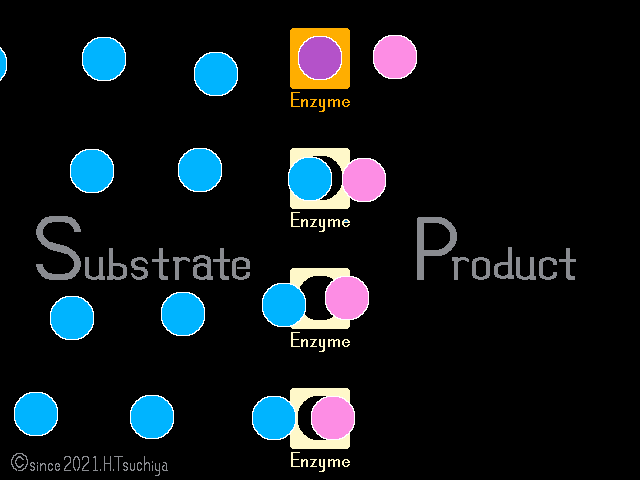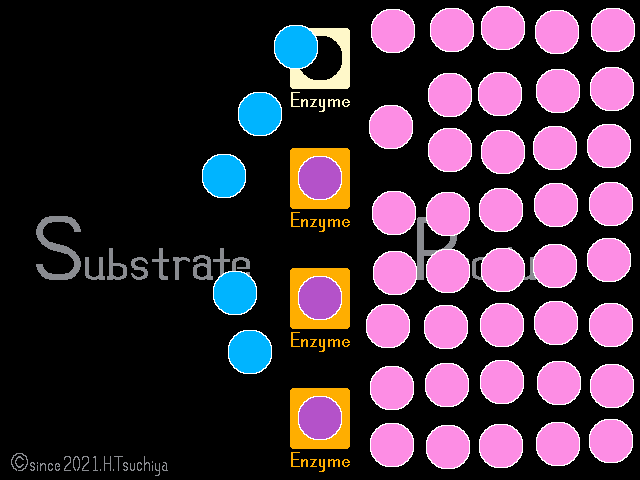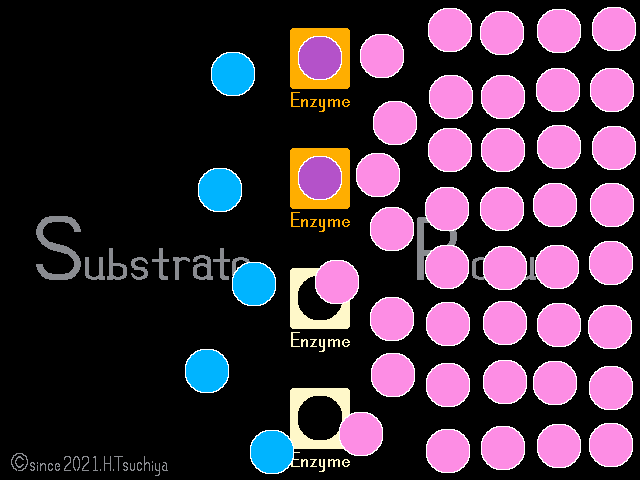
光合成や呼吸など、実際の生体内では、ある酵素反応の生成物は、次の酵素反応の基質として消費されることが多いので、個々の酵素反応が化学平衡に達することは少ない。
【補足】
- 代謝(生体内の化学反応。例えば”光合成“や”呼吸“など。)
- 触媒(化学反応を促進または抑制する物質。)
- 酵素(生体内ではたらく生体触媒。タンパク質を主成分としている。)
- 変性(加熱やpH変化などにより、タンパク質の立体構造が変化し、タンパク質の性質が変化すること。)
- 失活(酵素タンパク質が変性することで、触媒としての機能を失うこと。)
- 酵素-基質複合体(酵素の活性部位に、基質が結合した状態。)
- 基質特異性(それぞれの酵素タンパク質は特有の立体構造をもち、特に基質と結合する部分“活性部位”)
- 不可逆反応(燃焼反応や中和反応など、一方向にしか進まない化学反応。)
- 可逆反応(両方向に進む化学反応。)
【参考資料】
- 吉里勝利(2018).『改訂 高等学校 生物基礎』.第一学習社
- 浅島 誠(2019).『改訂 生物基礎』.東京書籍
- 吉里勝利(2018).『スクエア最新図説生物neo』.第一学習社
- 浜島書店編集部(2018).『ニューステージ新生物図表』.浜島書店
- 大森徹(2014).『大学入試の得点源 生物[要点]』.文英堂